疫情透視!醫師分析疫苗爭議解盲標準
【新唐人亞太台 2021 年 06 月 08 日訊】今天的疫情透視單元,請到前北榮感染科主治醫師鄭元瑜醫師。請教鄭醫師:國人相當關注,國產疫苗進度,中研院院士陳培哲指出,國產疫苗選了最難的技術去做研發,他說,美國身為蛋白質次單位疫苗的「一軍」,做完了臨床試驗都還沒辦法申請核准,身為二軍的台灣距離就更遠了。想請教您怎麼看?解盲過關與否的標準在哪?中央目前給國人的解釋是否清楚?
前北榮感染科主治醫師 鄭元瑜:「Novavax還沒有通過美國EUA的原因,是它的生產進度落後,其實從科學技術角度上來看,它的第二期和第三期臨床試驗的表現相當好,但是在這次的疫情發生之前,它剛好賣掉自己的工廠,之後所選擇的代工廠就在海外多個地方,所以在生產速度上受到影響,主要的生產地是這個印度血清研究所。印度又因為這個疫情突然大爆發,限制了疫苗對外輸出,也有一些海外工廠,受到美國對於疫苗製造的原材料,輸出海外的限制,這些問題後來都會有解決,也使得它的生產速度恢復。但中間還是落後,所以這都成了美國在EUA緊急授權給它的時候,進度就落後。
疫苗的研發確實是困難,台灣的公司有國光、高端和聯亞,剛好就是因為高端和聯亞由美國給予技術支援,有進入到第二期臨床試驗,那國光的話進度就不順利,這個蛋白質疫苗,蛋白質次單位疫苗,它的缺點是在緊急的疫情下,它需要比較長的研發時間,但是它的技術基礎安全性還有效果,其實都很好。目前我們有流感、B型肝炎、肺炎鏈球菌疫苗這些疫苗,都是屬於蛋白質次單位疫苗,那這個技術是有一定的門檻,台灣的發展是已經成熟了。
這個國產疫苗在解盲過關的標準,是保護力還有安全性。以高端疫苗最新的消息來看,他們對於自己第二期這個中途資料的分析結果,是滿有信心的,但是解盲的結果,還是要由第三方審核單位來做最後的判定,目前國產疫苗有優點就是說,中和抗體做出來效能是不錯,但是我們還不能確定,國際上最後會不會承認使用中和抗體來換算,對應成真實世界中疫苗對病毒的保護能力。這個叫做免疫橋接,還有就是因為臨床試驗人數原因,無法偵測出萬分之一等級的罕見副作用,這個問題是必須要說清楚,但是在嚴重的疫情之下,就算出現了這種萬分之一等級的罕見的不良反應,可能注射疫苗還是一個利大於弊的選擇。」
相關新聞
-

王必勝:自中國入境台灣須唾液PCR 監測變異株
2022-12-28 16:06:04中央流行疫情指揮中心今(28)日宣布,因應中國疫情升溫,為保障國人健康安全,及早發現確診者連結醫療照護,並防範及偵測高風險變異株,自明(112)年1月1日零時至1月31日(航班表定抵台時間),除維持現行不開放中國觀光客來台之政策外,搭乘自中國4個直航航線,及金馬地區民眾過年交通專案之來台旅客,入境時須於機場(或港口)配合採集唾液檢體進行PCR檢測,採檢後儘速返回住所進行7天自主防疫及後續自我篩檢,篩檢陽性者依規定進行5+n居家照護及自主健康管理,陽性檢體則後送疾管署昆陽實驗室進行病毒定序。
-

劇毒株肆虐 美重磅報告:武毒所洩漏釀大流行
2023-04-19 20:36:54歡迎回來。中共病毒大流行,遠未停歇。一種新冠病毒的變異毒株,又在全球多國肆虐。美國重磅報告直指,武漢實驗室的洩漏,導致了大流行。
-

確診中國旅客進入多國 未造成顯著疫情
2023-01-20 13:27:25中國疫情大爆發,中共當局對內對外完全躺平,大批檢測為陽性的旅客湧入海外,但是同一個病毒卻呈現不同影響,國際疫情依舊相當平穩,而在中國卻出現死亡潮,病毒學專家提出,人類應該謙卑反思。
-

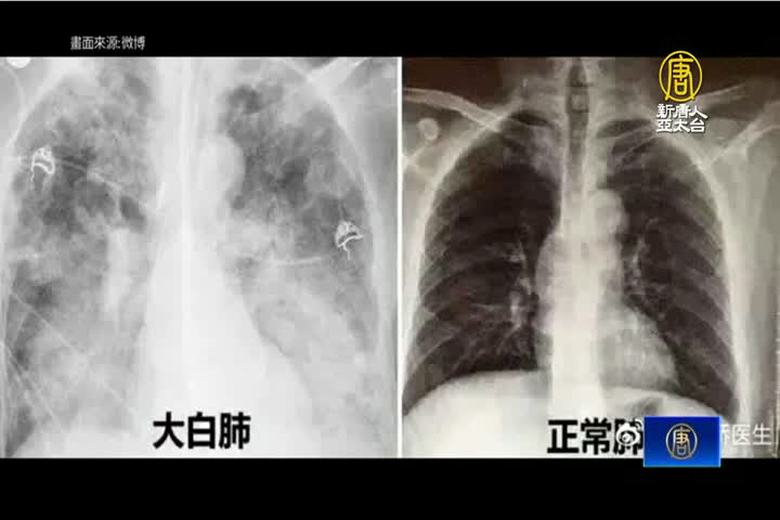
中共與天鬥清零失敗 陸網友轟「白肺心肌」
2023-01-03 16:38:54中共長達三年的清零封控失敗,現在疫情大爆發,出現「白肺」與「心肌炎」症狀的患者不斷蔓延至各個年齡層,有網友發文,家裡剛出生5天的新生兒,感染後遭醫院下病危通知書,右肺1/3出現白肺。由於中國本輪疫情中出現了大量「白肺」和「心肌炎」患者,中國網友更是創出了「白肺心肌」一詞,諷刺中共戰天鬥地的無效三年「清零」。目前,國際持續要求中共公布真實疫情數據,中國醫衛專家張文宏指出,過年期間,中國染疫比率可能高達80%,代表中國14億人口將有超過11億人染疫。
-

中國多地疫情頻現 官方承認「新冠沒有消失」
2023-03-23 20:31:55近日中國多地再現醫院發熱門診擠爆的情況。22日,「每日核酸陽性4000人以上」登上微博熱搜,中共專家承認「新冠沒有消失」。有中國民眾批評,疫情和流感何時爆發,嚴重程度如何,全是中共當局一手操縱。
-

火葬場排隊 常州15分鐘火化一具屍體
2023-01-20 20:48:04中共躺平式放開後,疫情衝擊波覆蓋全中國,死亡人數極速攀升。由於中共極力封鎖真相,有些民眾尚未察覺疫情的慘烈程度。
-

中國甲流迅速蔓延 學生測核酸引質疑
2023-03-09 16:41:41在中國大陸,疑似出現甲型流感(台灣稱A型流行性感冒)大面積爆發,不少確診者的症狀相當嚴重,疑似感染Covid-19中共病毒,還有很多孩童相繼中招。不少民眾懷疑,中共當局宣布了所謂的「防疫勝利」後,借著所謂甲流,繼續掩蓋Covid-19疫情。
-

韓日防疫降級 台最快今宣布室內免戴口罩
2023-01-31 11:52:45再來關心,全球受到COVID-19疫情肆虐已經第四年,除了中國大陸,各國疫情都有趨緩,重症及死亡的患者大量減少。韓國宣布30日起撤除室內口罩令,而日本則在日前宣布五月將會調降疫情等級。台灣也在週一,宣布開放的五大方向,如果和學者專家討論順利,最快今天週二,就會公布室內免戴口罩。
-

陸客尚未驗出新變種 醫觀察為何中國現死亡潮
2023-01-18 11:42:43中共掩蓋真實疫情,從當地醫院人滿為患,殯葬系統崩潰來看,外媒和專家學者都認為,中國死亡人數遠遠高出官方數字。而截至目前,從台灣中央流行疫情指揮中心公布的基因定序來看,中國仍是以BA.5跟BF.7為主,照理來說,重症跟致死率相對要弱,但為何會在中國造成殯葬與醫療系統的崩潰?來看醫師的分析。
-

甲流還是新冠?重症湧現 多名患兒不治離世
2023-03-11 20:11:18來關心中國疫情,甲流疫情,也就是A型流感,席捲中國近一個月,醫院爆滿,多地傳出重症患者,不幸去世的消息。民眾質疑,這到底是甲流,還是新冠?
-

陌生人變媽媽!中國疫情孤兒處境受關注
2023-01-20 13:19:45今天是小年夜,在中國大量民眾因為疫情逝去,最新曝光的一段影片,讓許多網友相當不捨,一名年紀約5、6歲的山東男孩,被收養在病房過年,把平時照顧他的一位阿姨叫媽媽。官方證實,這名男孩父母雙亡。
-

中國來台旅客採檢 學者估陽性率最高值35%
2023-01-02 16:34:46中國來台旅客唾液PCR採檢,首日陽性率27.8%。台大公衛學院教授陳秀熙今天說,數據在預期範圍內,反映中國疫情基本族群陽性率,估台灣未來檢出中國入境陽性率最高值35%。
-

2/7起入境自主防疫放寬 取消外出須快篩陰性
2023-02-02 11:48:52指揮中心今天公布,自2月7日起,調整入境旅客「0+7」自主防疫期間篩檢時機,取消外出須有2天內快篩陰性結果規範,改為自主防疫期間如出現症狀再使用家用快篩試劑篩檢。
-

新冠不斷變異 中國百姓情緒失控 怨聲載道
2023-04-21 20:58:49近日,中共官方宣稱,多種新冠變異毒株,已經在中國出現。有醫生透露,百姓情緒失控,對疫情感到厭煩和恐慌。
-

武肺甲流肆虐 中共強打針 權威揭驚人研究發現
2023-04-14 21:02:38中共當局再次推出強制接種疫苗要求,很多民眾表示不滿,並追問打針後遺症的資料和數據,與此同時,《美國醫學會期刊》的一項研究結果,令人擔憂。
-

甲流凶猛來襲 世衛又通報:江蘇婦女染禽流感
2023-03-03 21:10:47最近,在中國多地,所謂的「甲流」病毒,也就是台灣說的A型流感,還在流行,世衛又證實,禽流感傳人的最新病例,是來自中國江蘇的53歲婦女。多種病毒,在中國同時傳播。
-

「甲流」肆虐 南方進入流行高峰 多所中小學淪陷
2023-04-05 21:53:44中國大陸流感疫情捲土重來,廣東省再現流行高峰。近期,中國南方所謂的「甲流」A型流感患者明顯增多,中共官方承認,廣州有醫院的兒科門診,週末接診量高達平日的4倍。
-

北京市藥監局數據洩密 疫情嚴峻 民間一藥難求
2023-03-27 21:08:29「甲流」各地爆發,北京市藥監局的一個數據,間接證實了所謂的「甲流」疫情相當嚴峻,民間藥物需求量巨大,患者一藥難求。很多民眾懷疑,所謂的「甲流」,就是「新冠」換了個名字。
-

北京學生集中發熱 上海天津浙江多校緊急停課
2023-02-22 13:17:34鏡頭轉到中國,近日,從中國首都北京,到天津、上海等多地,都有學校傳出,學生出現發熱等症狀,暫時停課,雖然校方普遍宣稱是流感,但民間擔憂疫情會再度爆發。
-

台擬解除室內口罩令 CDC提醒陸疫情仍高峰
2023-01-17 11:52:14台灣防疫指揮官王必勝首度鬆口,如果台灣和國際疫情穩定,室內口罩令鬆綁,有望在過年後就實施,疫情降級也正在討論中。而即將進入過年連假,台灣指揮中心評估,中國大陸本土疫情仍嚴峻,已經從都市蔓延到鄉村,住院及死亡都處在高峰。